脂質ナノ粒子 Lipid Nanoparticles (LNPs) の作製
アプリケーション
脂質ナノ粒子(Lipid Nanoparticles: LNPs)
脂質ナノ粒子(LNP)は、臨床的に最も進んだ非ウイルス性遺伝子導入システムです。核酸脂質ナノ粒子により、核酸を安全かつ効果的に送達することができ、遺伝子医薬の開発やその使用に対する大きな障壁を克服することが可能となりました。
遺伝子医薬の用途には、遺伝子編集、迅速なワクチン開発、免疫腫瘍学、希少な遺伝性疾患や薬剤のない疾患の治療など、さまざまなものがありますが、これらはたいていにおいて核酸のデリバリーが課題となっています。
脂質ナノ粒子は、これまでの脂質ベースの核酸デリバリーシステムに比べ、以下のような利点を備えています。
- 高い核酸封入効率と高い導入効率
- 薬剤送達のための組織への浸透性が改善
- 細胞毒性、免疫原性が低い
上記により、脂質ナノ粒子は核酸デリバリー手段の有力候補となっています。脂質ナノ粒子を利用した最初のRNAi医薬品(Patisiran)は、2018年にFDAにより承認されました。
脂質ナノ粒子作製における課題の克服
| 既存の作製手法の課題 | NanoAssemblr®による解決 | |
| フォーミュレーションプロセスにバッチ間で深刻な変動がある | > | どのバッチでも再現性高く脂質ナノ粒子を作製できる |
| プロセスコントロールが限られ、脂質ナノ粒子が不均一である | > | 作製条件のコントロールにより、均質な脂質ナノ粒子が作製できる |
| 核酸の内包が十分でない | > | 高い核酸内包率をワンステップで実現できる |
| 作製に手間と時間がかかる | > | 手間なく即座に脂質ナノ粒子を作製できる |
| 製造プロセスのスケールアップが困難 | > | 製造におけるスケールアップはシームレスである |
特長
作製プロセスにおける高い再現性
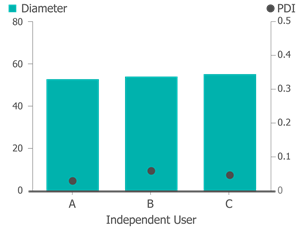
ユーザーが異なっても(ユーザーA・B・C)同じ材料であれば、脂質ナノ粒子のサイズは同じである。
作製条件が同じであれば、作製量に関わらず均一な脂質ナノ粒子製剤を実現
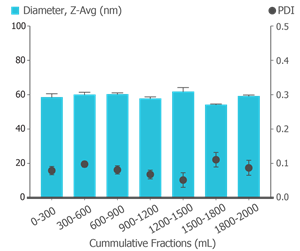
NanoAssemblr GMPシステムによる製造において、一貫したサイズおよびPDIのmRNA脂質ナノ粒子が全過程(0 – 2000mL)において作製された。
高い核酸内包率をワンステップフォーミュレーションプロセスで実現
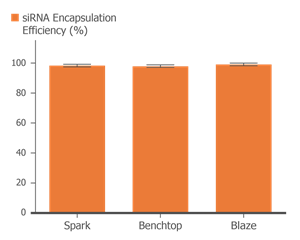
3種類のNanoAssemblr®装置でsiRNA-LNPsを作製したところ、いずれのsiRNA内包率も95%以上であった。
シームレスにLNP製造をスケールアップ
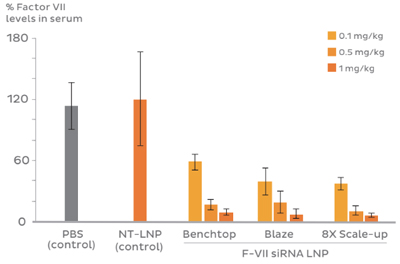
Factor VII siRNAノックダウン効果は、NanoAssemblr® Benchtop・Blaze・GMPシステムで作られたいずれのナノ粒子においても同様に維持されました。
NanoAssemblr®テクノロジーにより脂質ナノ粒子の特性が向上
より均質なナノ粒子を作るNanoAssemblr®プラットフォーム
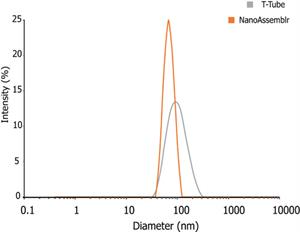
NanoAssemblr®プラットフォームで作った粒子は、今までのTチューブミキシング法で作った粒子よりも均質になります。
NanoAssemblr®による均質な構造のナノ粒子

Tチューブで作製した脂質ナノ粒子(左)は多重層形態を示す一方で、NanoAssemblr®で作製した脂質ナノ粒子(右)は均質なコア構造を示している。
NanoAssemblr®で作製した脂質ナノ粒子による優れたノックダウン効果
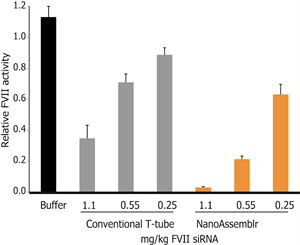
投与して72時間後において、NanoAssemblr®で作製したsiRNA脂質ナノ粒子は、Tチューブで作製したsiRNA脂質ナノ粒子よりも、高い血清第VII因子siRNAノックダウン効果を示した。
文献
エレクトロポレーション
■ 培養細胞
- 初代培養細胞
- iPS細胞・ES細胞・幹細胞
- オルガノイド
- 株化細胞
- 培養細胞(NEPA Porator)
- 付着状態の細胞
■ In Vivo・Ex Vivo マウス・ラット
- 受精卵(TAKE法)
- 受精卵(i-GONAD/r-GONAD法)
- In Utero胎児
- Ex Utero培養胚
- 脳・脳切片・培養脳組織
- 網膜・角膜・脊髄・坐骨神経
- 肺・脾臓・肝臓・腎臓・胃・腸
- 膵臓・ランゲルハンス島
- 精巣・卵巣・前立腺・生殖腺・子宮
- 筋肉・皮膚・関節・軟骨・腫瘍・その他
■ In Vivo・Ex Vivo その他の動物
- ウシ・ブタ・その他の動物の受精卵
- ハムスターi-GONAD法
- サル皮膚
- ニワトリ(In ovo・Ex ovo・他)
- ゼブラフィッシュ・その他の魚
- 両生類・昆虫・その他
■ 植物細胞・藻類
- 植物細胞
- 藻類
■ エクソソーム
- エクソソーム
■ バクテリア・酵母・菌類
- 大腸菌・バクテリア(細菌)
- 酵母・菌類
- 大腸菌・バクテリア・酵母・菌類(NEPA Porator)
ドラッグデリバリー・遺伝子導入
■ メカノポレーション
- 細胞治療
- 薬剤スクリーニング
■ ナノ粒子作製
- 概要
- 脂質ナノ粒子(LNPs)
- 脂質ナノ粒子 (LNPs) のスケールアップ
- リポソーム
- ポリマーナノ粒子
- T細胞への遺伝子導入
- 造血幹細胞への遺伝子導入
■ 超音波(ソノポレーション・FUS)
- 遺伝子導入の概要
- 脳
- 肝臓・皮膚・その他
- 心臓
- 培養細胞
- 肺
- 筋肉
■ ジェットインジェクション
- マウス・ラットの皮膚
■ パーティクルデリバリー
- 皮膚
- 植物
- 動物
■ マイクロインジェクション
- 植物細胞・藻類
電気式細胞融合
■ ハイブリドーマ作製
- モノクローナル抗体産生など
■ 卵子活性化
- 顕微授精(ICSI)の前・後の電気刺激など
■ 体細胞核移植
- クローン動物の作製
■ 四倍体胚の作出
- テトラプロイドキメラの作製など
■ その他
- リポソーム・プロトプラスト・酵母など
蛍光組織染色・in situ HCR
細胞分離
■ 幹細胞分取
- 幹細胞の分取・回収
- VIVANT-CELL®-Pot
1細胞回収・マイクロダイセクション
細胞凍結
細胞・微生物培養 (解析/計数/伸展/灌流)
■ 微生物計数カウント
- 真菌・酵母など
- 細菌
■ 微生物向けライブセルイメージング・解析
- 薬剤感受性試験
- 食品微生物学
- 作物学
■ 微生物汚染に対する品質管理・安全検査
- バイオバーデン試験
- 産業用水の試験
- 食品・飲料の試験
- 細胞培養
- 環境モニタリング
■ リアルタイム細胞解析
- 細胞増殖
- 細胞遊走・創傷治癒
- 細胞毒性
- 細胞バリア機能
- 細胞変性(ウイルス学)
■ 細胞計数分析
- 株化細胞
- 幹細胞
- 初代培養細胞
- バクテリア
- 酵母
- 藻類・原虫
- 血液関連細胞
- その他
- 実験例:細胞毒性評価
- 実験例:藻類摂食率測定
■ 細胞伸展培養
- メカノトランスダクション
- 遺伝子発現
- 細胞接着
- 伸展活性化チャネル
- ナノマテリアル
■ 細胞灌流培養
- 加圧培養
- 薬剤応答
- 細胞分化・長期
- 蛍光観察
In Vivo イメージング・モニタリング
■ バイタルサインモニタリング
- MARTA-Padバイタルサインの測定
■ 小動物用超音波イメージング
- 心血管研究
- 腫瘍・がん研究
- 汎用アプリケーション
- 発生生物学
- HIFU研究
- イメージガイドソノポレーション
- 弾性イメージング
卵振動培養
■ 卵子・胚盤胞
- 単為発生卵子および体細胞核移植胚 に由来する胚盤胞の効率的生産